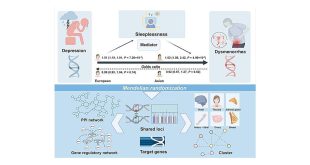
Недавнее исследование, опубликованное в журнале Molecular Psychiatry, свидетельствует о том, что хронический стресс может влиять на генетический материал спермы и, следовательно, на поведение потомства. Исследование показывает, что высокий уровень гормонов стресса разрушает длинные некодирующие РНК в сперматозоидах. Когда эти измененные РНК вводятся в оплодотворенные яйцеклетки, они приводят к изменениям в развитии и поведении, связанным с аффективными расстройствами, такими как тревожность и депрессия.
Исследователи решили изучить, как отцовский стресс перед зачатием влияет на поведение будущих поколений. Предыдущие исследования показали, что факторы окружающей среды, с которыми сталкиваются родители, могут влиять на поведение их потомства – явление, известное как эпигенетическое наследование. Ранее команда обнаружила, что связанные со стрессом изменения в малых некодирующих РНК (нкРНК) в сперматозоидах могут привести к усилению тревожного поведения у потомства мужского пола. Однако роль длинных некодирующих РНК в этом процессе оставалась неясной.
Малые некодирующие РНК представляют собой категорию молекул РНК, обычно длиной около 20–30 нуклеотидов, которые не кодируют белки, но играют решающую роль в регуляции экспрессии генов и поддержании стабильности генома. С другой стороны, длинные некодирующие РНК – это более длинные молекулы РНК длиной более 200 нуклеотидов, которые участвуют в различных клеточных процессах, включая ремоделирование хроматина, регуляцию экспрессии генов и модификацию других молекул РНК.
“Мы опубликовали исследование 8 лет назад (Short AK и соавт., 2016, Translational Psychiatry), показывающее, что повышенный уровень гормонов стресса вызывает изменения в малых некодирующих РНК в сперме мышей-отцов, а также изменения в тревожности и социальном поведении их потомства. Поэтому мы хотели изучить длинные некодирующие РНК и выяснить, могут ли эти изменения в РНК сперматозоидов способствовать изменениям в мозге и поведении потомства”, – объясняет автор исследования Энтони Ханнан из Института неврологии и психического здоровья Флори Мельбурнского университета
Исследование проводилось на мышах. Исследователи использовали мышей-самцов линии C57BL/6 из двух разных учреждений в Австралии. Мышей-самцов разделили на две группы: одна группа получала кортикостерон (гормон стресса) с питьевой водой в течение четырех недель, чтобы имитировать хронический стресс, а контрольная группа получала обычную питьевую воду.
После лечения исследователи собрали сперму у самцов и ее проанализировали с использованием метода CaptureSeq для выявления изменений в длинных некодирующих РНК.
Чтобы проверить влияние этих изменений, исследователи ввели длинные некодирующие РНК как из группы, получавшей кортикостерон, так и из контрольной группы, в оплодотворенные яйцеклетки мышей. Затем эти яйцеклетки имплантировали самкам мышей для производства потомства.
Потомство проходило различные поведенческие тесты для оценки тревожности, депрессии, социального доминирования и привлекательности. Тесты включали лабиринт “приподнятый плюс”, “светло-темную коробку”, тест на социальное доминирование в трубе, тест на выбор партнера и тест на принудительное погружение в воду (тест Порсолта).
Исследование показало, что воздействие кортикостерона привело к значительным изменениям в профиле длинных некодирующих РНК сперматозоидов. Из 7552 длинных некодирующих РНК 2382 были экспрессированы по-разному, причем 772 имели повышенную экспрессию, а 1610 – пониженную. Эти изменения включали альтерацию в специфических длинных некодирующих РНК, которые, как известно, участвуют в нейронной дифференцировке.
“Меня удивило, что так много (более 2000) различных крупных некодирующих РНК были изменены из-за повышения уровня гормонов стресса”, – говорит Ханнан.
Когда измененные длинные некодирующие РНК вводили в оплодотворенные яйцеклетки, у полученного потомства наблюдались заметные поведенческие различия. Потомство мужского пола из группы, получавшей микроинъекции, проводило больше времени в светлой зоне светло-темной коробки, что указывает на повышенную тревожность. Они также демонстрировали в большей степени депрессивное поведение в тесте принудительного плавания Порсолта, проводя больше времени в неподвижности по сравнению с контрольной группой.
Исследование также показало, что потомство, получившее микроинъекцию, имело увеличенную массу тела по сравнению с мышами, зачатыми естественным путем.
Это подчеркивает, что наличие дополнительных длинных некодирующих РНК может повлиять на физический рост в раннем взрослом возрасте.
“Эти результаты показывают, что повышенный уровень гормона стресса (моделирующего хронический стресс) может вызвать серьезные изменения в длинных некодирующих РНК в сперматозоидах, и что эти изменения могут способствовать изменению поведения потомства”, – объясняет Ханнан. “Эти изменения у потомства имеют отношение к депрессии и тревожным расстройствам. Нам необходимо знать, происходят ли эти изменения также в человеческой сперме и способствуют ли они нарушениям в работе мозга у следующего поколения”.
Исследование предоставляет убедительные доказательства связи отцовского стресса с изменениями в поведении потомства, но важно отметить, что исследование проводилось на мышах. Необходимы исследования на людях, чтобы определить, действуют ли подобные механизмы.
“Главное предостережение заключается в том, что наше исследование проводилось на мышах, и нам срочно нужно узнать, происходит ли это также в сперме человека”, – отметил Ханнан. “Но мы знаем, что сперма человека содержит аналогичный набор крупных некодирующих РНК. Мы также знаем, что содержание РНК в сперме человека может изменяться под воздействием окружающей среды, включая стресс”.
“Мы срочно хотим понять механизмы, которые задействуются, как до, так и после зачатия. Изучая эти механизмы на мышиных моделях, мы также хотим продолжить исследования на людях, включая долгосрочные когортные исследования с подробными данными о матерях, отцах и их детях”.
Понимание этих механизмов может иметь важные последствия, особенно для понимания наследуемости аффективных расстройств, таких как тревожность и депрессия.
Это направление исследований также оказывает более широкое влияние на наше понимание эволюции. Исследователи предполагают, что такие эпигенетические механизмы наследования могут быть адаптивной реакцией, позволяющей потомству лучше справляться с условиями окружающей среды, с которыми сталкиваются их родители.
“Такого рода исследования эпигенетического наследования имеют важные эволюционные последствия”, – говорит Ханнан. “Я предполагаю, что дарвиновская эволюция (которая протекает очень медленно и включает генетические мутации и естественный отбор на протяжении многих поколений) породила “ламаркистские механизмы”, которые позволяют передавать информацию об изменении воздействия окружающей среды по отцовской линии потомству, чтобы повысить адаптивную приспособленность следующего поколения”.
Помощь психолога
 Психологическая помощь новости психологии и психотерапии
Психологическая помощь новости психологии и психотерапии